


腫瘤ADC治療:
精準(zhǔn)抗癌的“生物導(dǎo)”
健康科普





在腫瘤治療領(lǐng)域,從傳統(tǒng)化療的 “無(wú)差別攻擊” 到靶向治療的 “精準(zhǔn)打擊”,醫(yī)學(xué)技術(shù)始終在追求更高的療效與更低的毒副作用。而抗體藥物偶聯(lián)物(Antibody-Drug Conjugate,ADC) 的出現(xiàn),更是將這種 “精準(zhǔn)性” 推向了新高度,被業(yè)界稱為抗癌的 “生物導(dǎo)彈”。那么,究竟該如何看待腫瘤 ADC 治療?它的核心優(yōu)勢(shì)是什么?當(dāng)前臨床應(yīng)用處于什么階段?又面臨哪些挑戰(zhàn)?本文將從多個(gè)維度展開(kāi)解析。
1
ADC 治療的核心原理:為何被稱為 “生物導(dǎo)彈”?
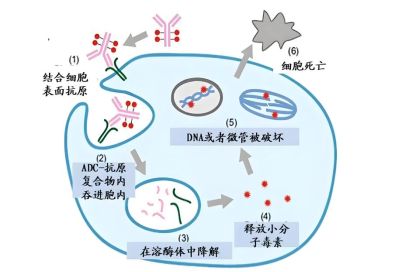
要理解 ADC 治療,首先需要拆解其 “三位一體” 的結(jié)構(gòu) ——單克隆抗體(導(dǎo)彈的 “導(dǎo)航系統(tǒng)”)、細(xì)胞毒性藥物(導(dǎo)彈的 “彈頭”)、連接子(連接導(dǎo)航與彈頭的 “橋梁”),三者協(xié)同作用實(shí)現(xiàn)對(duì)腫瘤細(xì)胞的精準(zhǔn)殺傷:
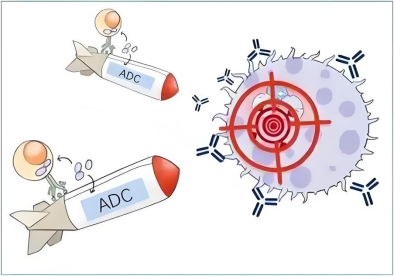
單克隆抗體會(huì)特異性結(jié)合腫瘤細(xì)胞表面過(guò)度表達(dá)的抗原(如 HER2、CD20、TROP2 等),就像導(dǎo)彈的導(dǎo)航儀一樣,能精準(zhǔn)識(shí)別腫瘤細(xì)胞并與之結(jié)合,避免對(duì)正常細(xì)胞的誤判,這是 ADC “精準(zhǔn)性” 的核心基礎(chǔ)。例如,針對(duì) HER2 陽(yáng)性乳腺癌的 ADC 藥物,其抗體部分可精準(zhǔn)鎖定乳腺癌細(xì)胞表面的 HER2 蛋白,確保藥物向腫瘤組織富集。
ADC 攜帶的 “彈頭” 多為高效的細(xì)胞毒性藥物(如微管抑制劑、DNA 損傷劑等),這類藥物的殺傷活性遠(yuǎn)高于傳統(tǒng)化療藥(通常是 10-1000 倍),但由于毒性極強(qiáng),單獨(dú)使用會(huì)對(duì)正常組織造成嚴(yán)重?fù)p傷。而 ADC 通過(guò)抗體的靶向遞送,讓 “彈頭” 只在腫瘤細(xì)胞內(nèi)釋放,既放大了殺傷效果,又降低了對(duì)全身正常細(xì)胞的毒性。
連接子是 ADC 的 “隱形關(guān)鍵”:它需要在血液中保持穩(wěn)定(避免 “彈頭” 提前脫落導(dǎo)致全身毒性),同時(shí)在 ADC 進(jìn)入腫瘤細(xì)胞后快速斷裂,釋放出 “彈頭” 藥物。目前臨床應(yīng)用的 ADC 多采用 “可裂解連接子”,平衡了安全性與有效性——例如某些連接子可在腫瘤細(xì)胞內(nèi)的酸性環(huán)境或特定酶的作用下裂解,進(jìn)一步提升靶向性。

簡(jiǎn)單來(lái)說(shuō),ADC 的作用機(jī)制是:抗體帶 “彈頭” 找到腫瘤→進(jìn)入腫瘤細(xì)胞→釋放 “彈頭” 殺死癌細(xì)胞→正常細(xì)胞幾乎不受影響,這也是它區(qū)別于傳統(tǒng)化療和普通靶向藥的核心優(yōu)勢(shì)。
2
ADC 治療的發(fā)展:從 “初代” 到 “新一代”,療效與安全性持續(xù)升級(jí)
ADC 并非全新技術(shù),其發(fā)展已歷經(jīng)數(shù)十年,大致可分為三個(gè)階段,每一代的進(jìn)步都圍繞 “提升療效、降低毒性” 展開(kāi):
代表藥物為 2000 年獲批的利妥昔單抗 - 伊達(dá)比星(Zevalin) 和 2001 年獲批的吉妥珠單抗 - 奧唑米星(Mylotarg)。這一代 ADC 的抗體靶向性較弱、連接子穩(wěn)定性差(易提前釋放藥物導(dǎo)致骨髓抑制等毒性)、“彈頭” 藥物活性有限,臨床應(yīng)用范圍較窄(僅用于部分淋巴瘤、急性髓系白血病),且部分藥物因毒性問(wèn)題曾短暫退市(如 Mylotarg),反映出初代技術(shù)的局限性。
隨著抗體工程、連接子化學(xué)和 “彈頭” 藥物的升級(jí),二代 ADC 實(shí)現(xiàn)了質(zhì)的飛躍,代表藥物包括曲妥珠單抗 - 美坦新偶聯(lián)物(T-DM1,2013 年獲批) 和恩美曲妥珠單抗(DS-8201a,2019 年獲批)。這一代 ADC 的核心進(jìn)步的是:
■ 抗體靶向性更強(qiáng)(如針對(duì) HER2 的曲妥珠單抗親和力更高);
■ 連接子更穩(wěn)定(血液中藥物脫落率降低,毒性顯著下降);
■ 引入 “載荷優(yōu)化”(每個(gè)抗體可攜帶更多 “彈頭” 藥物,提升殺傷效率)。
以 T-DM1 為例,它成為 HER2 陽(yáng)性乳腺癌的二線治療標(biāo)準(zhǔn),相比傳統(tǒng)化療,將中位無(wú)進(jìn)展生存期(PFS)從 6.4 個(gè)月延長(zhǎng)至 9.6 個(gè)月,且腹瀉、嘔吐等副作用發(fā)生率降低 50% 以上;而 DS-8201a 更是憑借 “旁觀者效應(yīng)”(釋放的 “彈頭” 可殺傷鄰近未被抗體結(jié)合的腫瘤細(xì)胞),對(duì) HER2 低表達(dá)乳腺癌也有效,進(jìn)一步擴(kuò)大了適用人群。
當(dāng)前 ADC 已進(jìn)入 “多靶點(diǎn)、多癌種” 的爆發(fā)期,除了 HER2,新靶點(diǎn)如TROP2(針對(duì)乳腺癌、肺癌)、Claudin 18.2(針對(duì)胃癌、胰腺癌)、CD19(針對(duì)淋巴瘤、白血病)、Nectin-4(針對(duì)尿路上皮癌) 等不斷涌現(xiàn),適應(yīng)癥從乳腺癌、淋巴瘤擴(kuò)展到肺癌、胃癌、胰腺癌、尿路上皮癌等十多種實(shí)體瘤和血液腫瘤。例如,2022 年獲批的戈沙妥珠單抗(SG,針對(duì) TROP2) 為三陰性乳腺癌(傳統(tǒng)治療手段有限)提供了新選擇,將中位總生存期(OS)從 5.6 個(gè)月延長(zhǎng)至 11.8 個(gè)月;針對(duì) Claudin 18.2 的 ADC 藥物(如 ZW49)在晚期胃癌臨床試驗(yàn)中,客觀緩解率(ORR)達(dá)到 50% 以上,為耐藥患者帶來(lái)希望。
3
ADC 治療的核心優(yōu)勢(shì):相比傳統(tǒng)治療,它解決了哪些痛點(diǎn)?
在腫瘤治療中,傳統(tǒng)化療的最大問(wèn)題是 “敵我不分”—— 殺死癌細(xì)胞的同時(shí),也會(huì)損傷毛囊細(xì)胞(導(dǎo)致脫發(fā))、消化道黏膜細(xì)胞(導(dǎo)致惡心嘔吐)、骨髓細(xì)胞(導(dǎo)致白細(xì)胞降低),毒副作用讓很多患者難以耐受;而普通靶向藥(如小分子 TKI)雖靶向性強(qiáng),但易出現(xiàn)耐藥(如 HER2 陽(yáng)性乳腺癌患者使用曲妥珠單抗 1-2 年后可能耐藥),且對(duì)部分靶點(diǎn)(如 TROP2)缺乏有效藥物。ADC 治療則針對(duì)性解決了這些痛點(diǎn),核心優(yōu)勢(shì)可總結(jié)為三點(diǎn):

一方面,抗體的靶向性讓藥物在腫瘤組織中富集(濃度是正常組織的 10-100 倍);另一方面,“彈頭” 藥物的高活性可有效殺死癌細(xì)胞,即使是對(duì)傳統(tǒng)靶向藥耐藥的腫瘤也可能有效。例如,DS-8201a 在 HER2 陽(yáng)性乳腺癌耐藥患者中,ORR 達(dá)到 60% 以上,遠(yuǎn)高于傳統(tǒng)化療的 20%-30%。
由于 “彈頭” 藥物僅在腫瘤細(xì)胞內(nèi)釋放,正常細(xì)胞幾乎不接觸高毒性藥物,因此 ADC 的全身毒副作用(如骨髓抑制、消化道反應(yīng)、脫發(fā))顯著低于傳統(tǒng)化療。例如,戈沙妥珠單抗在三陰性乳腺癌治療中,3 級(jí)以上中性粒細(xì)胞減少發(fā)生率僅為 20%,遠(yuǎn)低于化療的 40%-50%;且?guī)缀醪粫?huì)導(dǎo)致脫發(fā),極大提升了患者的生活質(zhì)量。
對(duì)于傳統(tǒng)治療手段有限的腫瘤(如三陰性乳腺癌、晚期胰腺癌、尿路上皮癌),或靶點(diǎn)表達(dá)較低的腫瘤(如 HER2 低表達(dá)乳腺癌),ADC 也能發(fā)揮作用。例如,HER2 低表達(dá)乳腺癌占所有乳腺癌的 40%-50%,此前無(wú)針對(duì)性靶向藥,而 DS-8201a 的臨床試驗(yàn)顯示,這類患者使用后中位 OS 可達(dá) 17.5 個(gè)月,相比化療延長(zhǎng)近 6 個(gè)月,填補(bǔ)了治療空白。
4
ADC 治療的臨床應(yīng)用現(xiàn)狀:哪些患者適合?已有哪些藥物可用?
目前,全球已獲批的 ADC 藥物超過(guò) 20 種,國(guó)內(nèi)獲批的有 10 余種,主要覆蓋以下癌種和靶點(diǎn),患者可根據(jù)自身情況匹配:
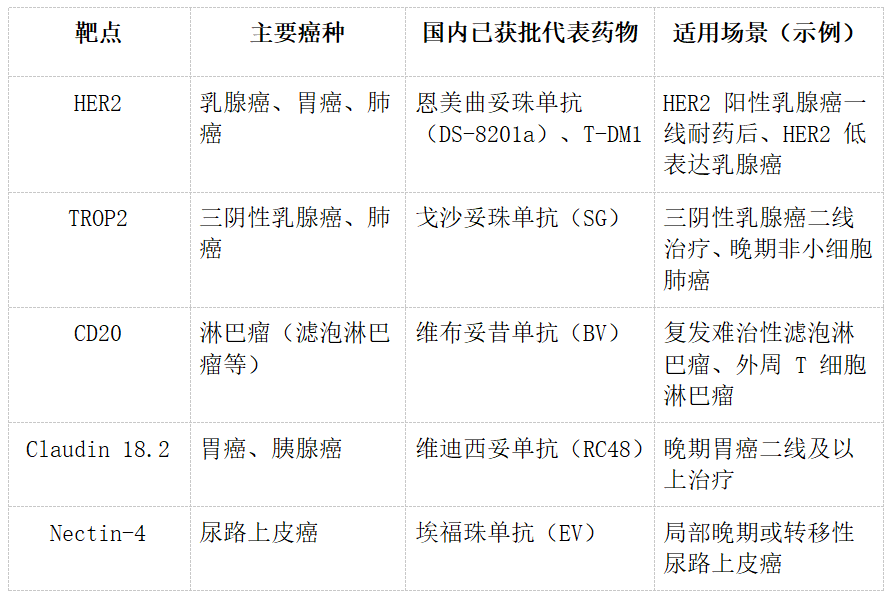
需要注意的是,ADC 治療并非 “萬(wàn)能藥”,患者需滿足兩個(gè)核心條件:
■ 腫瘤細(xì)胞表達(dá)對(duì)應(yīng)靶點(diǎn):需通過(guò)病理檢測(cè)(如免疫組化、FISH、NGS)確認(rèn)腫瘤細(xì)胞表面存在 ADC 針對(duì)的抗原(如 HER2 陽(yáng)性、TROP2 陽(yáng)性),這是使用 ADC 的前提;
■ 身體狀況允許:雖然 ADC 毒性較低,但仍可能存在一定副作用(如間質(zhì)性肺病、肝損傷),患者需經(jīng)醫(yī)生評(píng)估肝腎功能、心肺功能等,確保能耐受治療。
5
ADC 治療面臨的挑戰(zhàn):療效之外,還有哪些問(wèn)題待解決?
盡管 ADC 治療已取得顯著進(jìn)展,但在臨床應(yīng)用中仍面臨一些挑戰(zhàn),限制了其進(jìn)一步普及:

與其他靶向藥類似,ADC 也可能出現(xiàn)耐藥,主要原因包括:
①腫瘤細(xì)胞下調(diào)靶點(diǎn)表達(dá)(如 HER2 蛋白減少,抗體無(wú)法結(jié)合);
②腫瘤細(xì)胞激活耐藥通路(如通過(guò)泵蛋白將 “彈頭” 藥物排出細(xì)胞外);
③“彈頭” 藥物代謝加快(導(dǎo)致細(xì)胞內(nèi)藥物濃度不足)。
目前針對(duì)耐藥的解決方案仍在探索中,例如聯(lián)合免疫治療(如 PD-1 抑制劑)增強(qiáng)抗腫瘤效應(yīng),或開(kāi)發(fā)針對(duì)新靶點(diǎn)的 ADC 藥物。
雖然 ADC 全身毒性低,但部分藥物可能引發(fā)特定副作用,例如:
①DS-8201a 可能導(dǎo)致間質(zhì)性肺病(發(fā)生率約 10%,嚴(yán)重時(shí)可致命);
②維布妥昔單抗可能引發(fā)周圍神經(jīng)病變(發(fā)生率約 30%,表現(xiàn)為手腳麻木);
③多數(shù) ADC 可能導(dǎo)致血小板減少(因骨髓造血功能受輕微影響)。
這些副作用需要在治療過(guò)程中密切監(jiān)測(cè),及時(shí)調(diào)整劑量或停藥。
由于 ADC 的研發(fā)成本高(涉及抗體、連接子、“彈頭” 的多環(huán)節(jié)優(yōu)化),目前部分藥物價(jià)格較高,例如 DS-8201a 每月治療費(fèi)用約2-3萬(wàn)元,雖已納入部分地區(qū)醫(yī)保,但仍有患者因經(jīng)濟(jì)原因無(wú)法使用。未來(lái)隨著國(guó)產(chǎn) ADC 藥物的研發(fā)(如國(guó)產(chǎn) Claudin 18.2 ADC)和醫(yī)保覆蓋范圍擴(kuò)大,價(jià)格問(wèn)題有望逐步緩解。
目前 ADC 的靶點(diǎn)主要集中在 HER2、TROP2、CD20 等少數(shù)抗原,而對(duì)于一些 “無(wú)明確靶點(diǎn)” 的腫瘤(如部分胰腺癌、肝癌),仍缺乏對(duì)應(yīng)的 ADC 藥物。未來(lái)需要通過(guò)基因測(cè)序、蛋白質(zhì)組學(xué)等技術(shù),發(fā)現(xiàn)更多腫瘤特異性靶點(diǎn),擴(kuò)大 ADC 的適用范圍。
6
ADC 治療的未來(lái)方向:技術(shù)創(chuàng)新將帶來(lái)哪些突破?
從當(dāng)前研發(fā)趨勢(shì)來(lái)看,ADC 治療正朝著 “更精準(zhǔn)、更安全、更廣泛” 的方向發(fā)展,未來(lái)可能出現(xiàn)以下突破:

傳統(tǒng) ADC 僅針對(duì)單一靶點(diǎn),而雙靶點(diǎn) ADC(同時(shí)結(jié)合兩個(gè)腫瘤抗原,如 HER2+TROP2)可進(jìn)一步提升對(duì)腫瘤細(xì)胞的識(shí)別精度,減少正常細(xì)胞的誤結(jié)合,同時(shí)降低因單一靶點(diǎn)下調(diào)導(dǎo)致的耐藥風(fēng)險(xiǎn)。目前已有雙靶點(diǎn) ADC 進(jìn)入臨床試驗(yàn)(如 HER2+CD46 ADC),初步數(shù)據(jù)顯示療效優(yōu)于單靶點(diǎn) ADC。
未來(lái)的連接子將更加 “智能”—— 不僅能在腫瘤細(xì)胞內(nèi)裂解,還能根據(jù)腫瘤微環(huán)境的特定信號(hào)(如高濃度的乳酸、特定酶)觸發(fā)藥物釋放,進(jìn)一步提升藥物在腫瘤組織的濃度,降低全身毒性。例如,針對(duì)腫瘤酸性環(huán)境(pH 值低)的“pH 敏感型連接子”,已在臨床前研究中顯示出良好的安全性。
目前“彈頭”藥物多為傳統(tǒng)化療藥的衍生物,未來(lái)可能引入新型殺傷機(jī)制的藥物,如 “免疫刺激性彈頭”(釋放后可激活患者自身免疫系統(tǒng),增強(qiáng)抗腫瘤效應(yīng))、“基因毒性彈頭”(直接破壞腫瘤細(xì)胞 DNA,且不易耐藥)。例如,部分研發(fā)中的 ADC 采用 “雙彈頭” 設(shè)計(jì)(同時(shí)攜帶細(xì)胞毒性藥物和免疫刺激劑),可實(shí)現(xiàn) “殺傷 + 免疫激活” 的雙重作用。
ADC 與免疫治療(如 PD-1/PD-L1 抑制劑)的聯(lián)合是當(dāng)前的研究熱點(diǎn):ADC 殺死癌細(xì)胞后,會(huì)釋放腫瘤抗原,激活免疫系統(tǒng),而免疫治療可進(jìn)一步增強(qiáng)免疫細(xì)胞對(duì)腫瘤的攻擊,形成 “1+1>2” 的協(xié)同效應(yīng)。例如,DS-8201a 聯(lián)合 PD-1 抑制劑在 HER2 陽(yáng)性肺癌中的臨床試驗(yàn)顯示,ORR 達(dá)到 70% 以上,遠(yuǎn)高于單獨(dú)使用 ADC 的 50%。此外,ADC 與放療、小分子靶向藥的聯(lián)合也在探索中,有望進(jìn)一步提升療效。
7
總結(jié):如何理性看待 ADC 治療?
ADC 治療無(wú)疑是腫瘤精準(zhǔn)治療領(lǐng)域的重大突破,它以 “精準(zhǔn)殺傷、低毒高效” 的優(yōu)勢(shì),為眾多難治性腫瘤患者帶來(lái)了新希望,尤其是在 HER2 陽(yáng)性乳腺癌、三陰性乳腺癌、晚期胃癌等領(lǐng)域,已改變了臨床治療格局。但我們也需理性認(rèn)識(shí)到,ADC 并非 “抗癌神藥”——它仍存在耐藥、特定副作用、價(jià)格較高等問(wèn)題,且并非所有患者都適合(需靶點(diǎn)陽(yáng)性)。
對(duì)于患者而言,看待 ADC 治療的核心邏輯是:先檢測(cè)靶點(diǎn),再評(píng)估身體狀況,最后結(jié)合經(jīng)濟(jì)條件選擇——若腫瘤表達(dá)對(duì)應(yīng)靶點(diǎn)(如 HER2、TROP2),且身體能耐受治療,ADC 可作為優(yōu)先考慮的方案之一;若靶點(diǎn)陰性或存在嚴(yán)重基礎(chǔ)疾病,則需選擇其他治療手段(如化療、免疫治療、小分子靶向藥)。

從行業(yè)視角來(lái)看,隨著靶點(diǎn)探索的深入、技術(shù)的持續(xù)升級(jí)(如雙靶點(diǎn) ADC、智能連接子)以及國(guó)產(chǎn)藥物的崛起,ADC 治療未來(lái)將更廣泛地應(yīng)用于臨床,有望成為更多腫瘤的 “標(biāo)準(zhǔn)治療”。相信在不久的將來(lái),ADC 將與免疫治療、基因治療等技術(shù)協(xié)同,為腫瘤患者帶來(lái)更長(zhǎng)期的生存獲益和更高的生活質(zhì)量。

END
供稿 | 腫瘤科一病區(qū) 董利
編輯 | 井 靜
初審 | 張 暉
復(fù)審 | 李偉琳
終審 | 崔建國(guó)
(部分圖片來(lái)源于網(wǎng)絡(luò),如有侵權(quán)請(qǐng)告知?jiǎng)h除)






